Ley de la conservación de la masa o de Lavoisier – Química 2
Uno de los fenómenos más observados por los seres humanos desde el descubrimiento del fuego es a combustión, este descubrimiento se realizó hace más de un millón de años
Haciendo un poco de historia, el Homo ergaster llegó a conocerlo por casualidad y buscó cómo preservarlo
El objetivo principal o lo importante era la utilidad material del fuego, pero luego trascendió como objeto de conocimiento humano a nivel de la cosmología
Aproximadamente, hace unos 2 500 años, los griegos se planteaban preguntas como:
-¿Por qué razón algunos cuerpos pueden arder mientras que otros no lo hacen?
Esta cultura y sus razonamientos suponían que todo lo que podía entrar en combustión llevaba dentro de sí el elemento fuego y que este se liberaba bajo condiciones apropiadas
Los alquimistas, antecesores del conocimiento químico, pensaban de manera semejante:
-Las sustancias combustibles poseían el “principio de azufre” que les permitía tal capacidad
En el año 1702, Georg Ernest Stahl, médico y químico alemán, presentó la denominada teoría del:
De acuerdo con esta teoría, el flogisto o principio inflamable era una sustancia imponderable, misteriosa, que formaba parte de los cuerpos combustibles
Sin embargo fue Lavoisier quien demostró la inexistencia del flogisto mediante experimentos donde cuidadosamente midió la masa de las sustancias antes, durare y después de la combustión.
Gracias a sus experimentos, Lavoisier sentó las bases de la química moderna al incorporar a la observación herramientas para medir cuidadosamente lo que sucede durante el proceso de los fenómenos químicos.
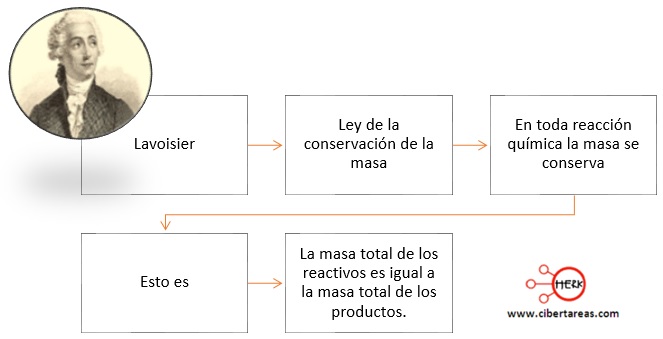
Lavoisier logró enunciar la importante ley de la conservación de le masa: