Modos de calcular la concentración de una disolución, molaridad – Química 2
La molaridad (M) de una solución se define como:
 Los moles de una sustancia se obtienen al dividir la masa de la muestra entre la masa molar o masa atómica, según sea un compuesto o un elemento, respectivamente
Los moles de una sustancia se obtienen al dividir la masa de la muestra entre la masa molar o masa atómica, según sea un compuesto o un elemento, respectivamente
Si se sustituye la ecuación numero 2 por la variable “n” de la ecuación 1, tenemos:
Aplicando la regla del sándwich, en la que se multiplica extremo por extremo y medio por medio tenemos:
Caso 1
¿Cuántos gramos de NaOH son necesarios para preparar 450 mL de solución 0.25M?
Solución:
Datos:
M = 0.25 m/L
M = ?
MMNaOH = 39.98 g/mol
V = 450 mL = 0.45 L
Para poder llegar a la solución es necesario tomar como punto de partida la ecuación numero 4
Después se despeja la variable “m” y finalmente se sustituyen los datos para cada una de las variables presentes, entonces tenemos:
Caso 2
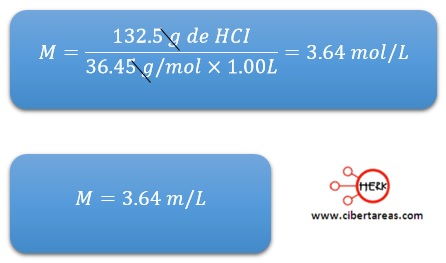
Se disuelven 132.5 g de ácido clorhídrico (HCI) en agua suficiente hasta obtener 1.00 L de solución, es necesario calcular su molaridad (M)w
Solución:
Datos
M = 132.5 g
MMHCI = 36.45 g/mol


David Vásquez says:
La ecuación 2 es incorrecta: n = m/MM y
en el despeje de la ecuación 4 en el ejercicio llamado “caso 1” faltó la M de molaridad