El modelo atómico de Rutherford – Química 1
Como sabemos, muchos de los grandes descubrimientos que se han dado en la humanidad, has sido de manera accidental, entre estos grandes descubrimientos tenemos la radiactividad.
Henri Becquerel (físico francés) realizo un experimento buscando la posibilidad de que los rayos X emitieran fluorescencia, para esto, coloco trozos de material fluorescente sobre placas fotográficas, estas placas estaba cubiertas con papel negro, las expuso a la luz solar para determinar si se velarían estas placas aun con su cubierta protectora, lo que encontró es que efectivamente después de estar expuestas durante cierto tiempo a la luz solar, estas placeas se velaba.
De casualidad, entre los materiales fluorescentes Henri coloco sales de uranio con esto las placas se velaron aunque los días estuvieran nublados o estuvieran guardadas en un lugar son luz, como en un cajón.
Después de varias pruebas se demostró que las sales de uranio emitían radiaciones desconocidas, a este fenómeno se le denomino Radiactividad.
Años después, el matrimonio de Marie Curie y Pierre, con sus experimentos descubrieron los elementos radiactivos, el radio y polonio, en sus descubrimientos reconocieron que la radiactividad es de naturaleza atómica.
Tiempo después, Ernest Rutherford estaba experimentado con los rayos X y descubrió otro tipo de emisiones:
Realizo la siguiente clasificación de los rayos:
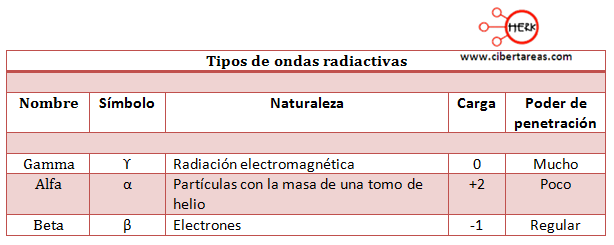
Tenemos las siguientes características:
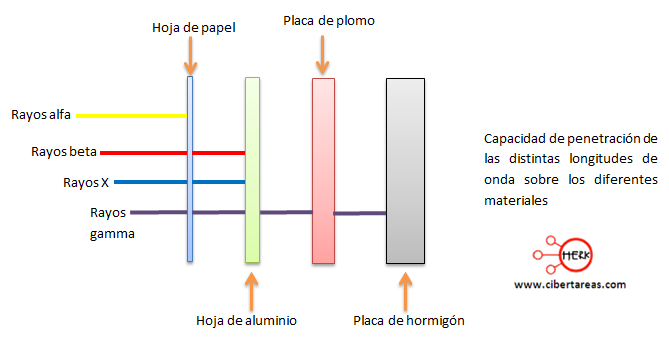
Los rayos alfa son poco penetrantes y estos pueden ser detenidos por una hoja de papel.
Los rayos Beta son más penetrantes y estos pueden atravesar una hoja de aluminio de 0.3 mm de espesor.
Los rayos Gamma tienen mayor poder de penetración, ya que son capaces de atravesar placas gruesas de metal como el plomo de 3 mm de espesor.
Rutherford con sus experimentos demostró que los rayos alfa eran sensibles a los campos magnéticos y eléctricos, entonces pudo determinar la relación carga-masa, tal y como lo hizo Thomson con el electrón.
Rutherford elabora un experimento en el que busca explorar el interior de un átomo, para esto emplea una fuente radiactiva de rayos alfa, con la cual bombardea a una lámina delgada de oro de 0.0006 mm de espesor.
Detrás de la lámina coloca una placa de sulfuro de zinc que emite luz cuando es alcanzada por los rayos alfa, después de varias pruebas se encontró que:
La mayor parte de la radiación había atravesado la placa de oro.
Algunas se desviaron en ángulos pequeños
Muy pocas rebotaron hacia la fuente de energía radiactiva.
Estos resultados no concordaban en el modelo propuesto por Thomson, quien decía en su modelo que el átomo era una masa más densa de protones y electrones.
El modelo atómico que Rutherford propuso señala que:
Con este modelo, Rutherford propone: