Isomería en Temas Selectos de Química 2
Tenemos que saber que cuando se tienen dos o más compuesto con la misma fórmula molecular, pero cuyos átomos se encuentran distribuidos de distintas formas, se llaman isómeros, este arreglo diferente de los átomos le confiere a cada isómero propiedades físicas y químicas que dependen del tipo de isomería:
-Isómeros estructurales
-Presentan enlaces distintos
-Estereoisómeros
-De iguales enlaces pero arreglo espacial diferente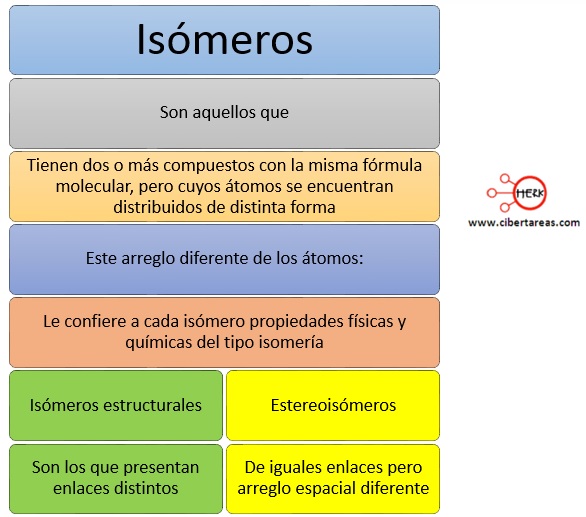
Dentro de los estereoisómeros, tenemos:
-Isómeros ópticos
-Llamados también enantiómeros (del griego enantios: opuestos)
Existen muchos compuestos cuyas moléculas, aunque tengan igual composición química (formula global) se puede presentar en dos formas ópticas diferentes, cada una de las cuales es la imagen especular de la otra, lo que se conoce como quirilidad
Molécula quiral
-La molécula quiral se presenta cuando no se superpone con su imagen especular
-Las dos formas de una molécula quiral se denomina isómeros ópticos o enantiómeros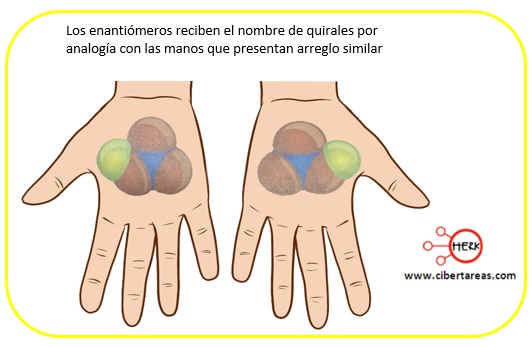
Molécula aquiral
-Son aquellas moléculas que se superponen con su imagen
Hay que considerar que los isómeros ópticos e enantiómeros se relacionan del mismo modo que n objeto y su imagen en el espejo, por ejemplo:
-El grupo –CH3 de uno refleja la posición del grupo –CH3 del otro, el –OH refleja al –OH
Lo anterior se puede representar cuando se coloca un espejo ante el guante de la mano derecha, lo que se refleja es la imagen del guante de la mano izquierda
Los isómeros ópticos tiene exactamente las misma propiedades químicas y físicas, sin embargo en el organismo cada enantiómero de un compuesto quiral puede ejercer una acción diferente en cuanto a la actividad biológica, toxicidad, metabolismo, etc.
Entonces se aconseja realizar la obtención por separado de cada enantiómero puro de un fármaco
Para saber si una molécula es quiral o no, se considera su plano de simetría, un plano de simetría divide a un objeto o una molecular de manera longitudinal, de tal forma que una parte de la estructura queda como imagen especular de la otra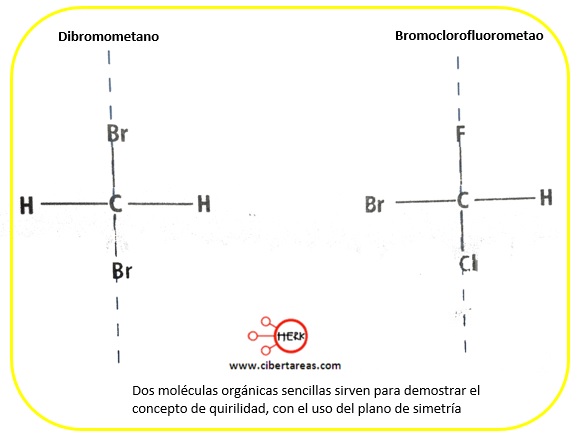
Dibromometano
-Presenta plano de simetría
-Este plano se representa en la figura anterior por la línea punteada
-Una parte de la molécula es la imagen especular de la otra
Bromoclorofluorometao
-No tiene plano de simetría
-Ninguna parte de la molécula es la imagen especular de la otra
Debemos saber que algunos objetos o moléculas pueden presentar más de un plano de simetría, lo cual torna complicado utilizar el criterio este criterio como único para definir si una molécula es quiral o no
Entonces tenemos que el primer criterio a emplear para considerar quiral o no a una molécula u objeto, es la superposición de tal molécula con su imagen especular
Sin embargo, al halar de la moléculas orgánicas, el criterio de quirilidad mas comuna, es la presencia de un átomo de carbono unido a cuatro átomos o grupos distintos. A tal átomo se le dan los siguientes nombres:
-Carbono asimétrico
-Centro asimétrico o centro quiral (que no tiene simetría)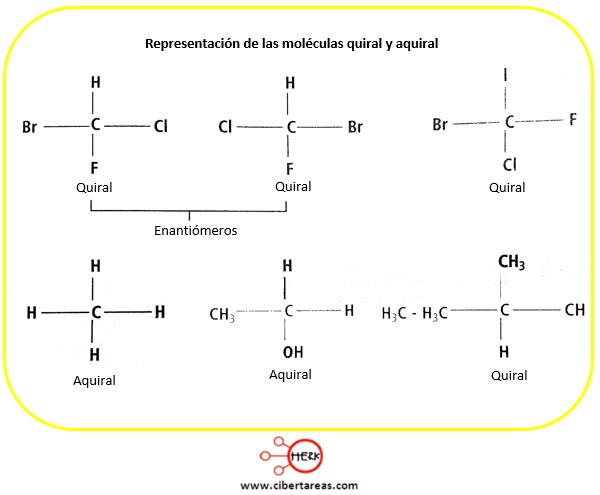
Hay que considerar que toda molécula que presente al menos un centro quiral será siempre quiral
Si se considera a los dos carbohidratos más simples, el gliceraldehido (aldotriosa) y la dihidroxiacetona (cetotriosa), el primero es un único que presenta enantiómeros y tiene quirilidad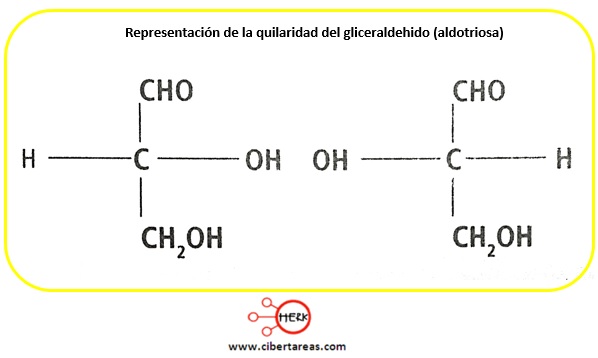
Al observar ambas moléculas se puede ver una gran similitud entre ellas, así como la poca diferencia en sus propiedades, para poder distinguir una de otra se tiene que los enantiómeros guardan una relación especial con la luz
Al aislarse cada enantiómero de forma pura es muy difícil distinguir uno de otro debido a que presentan propiedades físicas muy similares, como:
-Punto de ebullición
-Densidad
Lo anterior se da ya que sus enlaces son idénticos y su contenido energético muy similar
Sin embargo al hacerlos pasar por luz polarizada en un plano por una muestra de uno de los enantiómeros, la luz reaccionara con los electrones de los distintos enlaces de la molécula de tal manera que la interacción entre la luz (campo magnético) y la molécula será distinta en su parte izquierda y derecha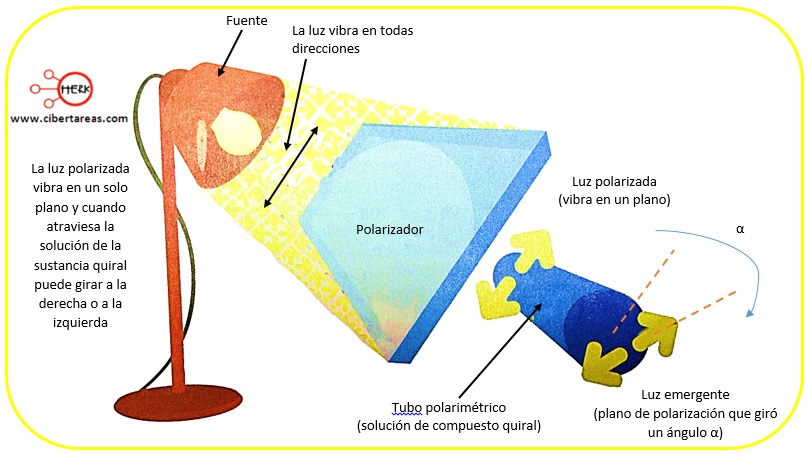
Dextrógiro
-Cuando un enantiómero hace girar el plano de la luz polarizada hacia la derecha, en el sentido de las manecillas del reloj, en relación con un observador que mira la fuente de luz
-La palabra dextrógiro proviene del latín dexterm que significa derecha
-Se puede simbolizar convencionalmente como (+)
Levógiro
-Cuando un enantiómero debía la luz polarizada hacia la izquierda
-Proviene del latín laevus, que significa izquierda
-Se identifica como (-)
De una manera fácil, a nivel práctico se pude definir, mediante una muestra del carbohidrato, la diferencia ente un enantiómero y otro, con la simple observación del sentido hacia donde se desvía la luz polarizada
En primer lugar, existen diversas formas de representar una molécula, pero para fines prácticos se emplean estructuras básicas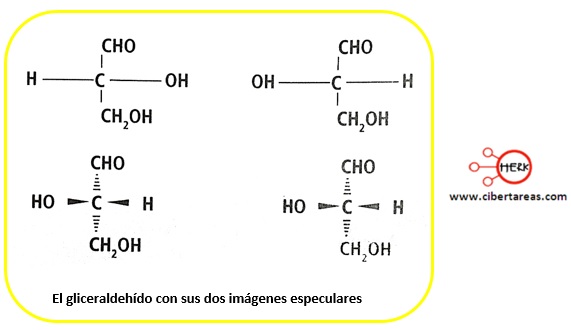
La primera representación muestra los enlaces del carbono con sus respectivos grupos en un plano unidimensional
La segunda, conocida corno proyección de Fischer, es una perspectiva bidimensional (trazos y cuñas), donde los enlaces que se representan en forma horizontal señalan su dirección hacia el frente del observador de la estructura y los que se aparecen en forma vertical representan enlaces dirigidos hacia atrás
Por otro lado, los carbonos se numeran desde la parte superior y de manera secuencial, como se parecía: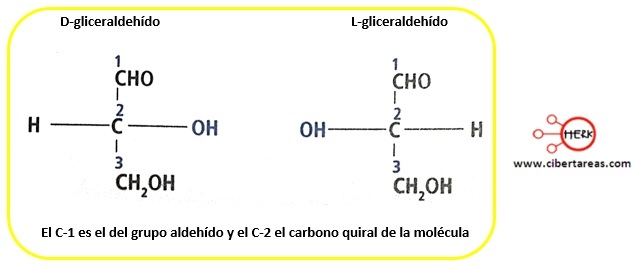
Es importante observar el carbono quiral, responsable del carácter de enantiómero de la molécula, la diferencia se encuentra en la ubicación del -OH del carbono quiral, pues en la primera estructura se encuentra a la derecha y en la segunda a la izquierda
A partir de esta característica se designa a la estructura una configuración D si el -OH se encuentra a la derecha del carbono quiral y L si se encuentra a la izquierda
Hay que considerar que se aplica la misma regla en estructuras más grandes, peor bajo condiciones diferentes, como las aldosas son azúcares más comunes que las cetosas, tenemos la estructura de la glucosa, el monosacárido más importante: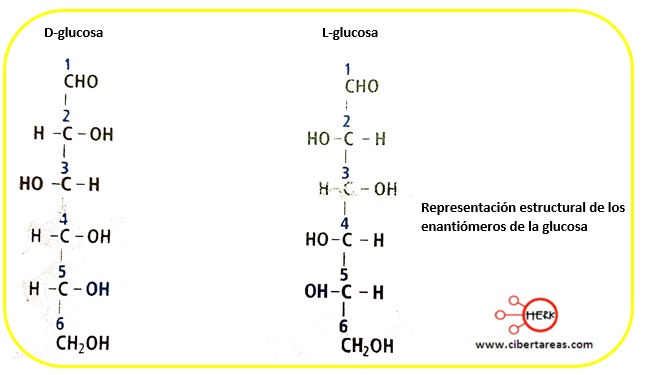
Para moléculas más grandes que el gliceraldehído, la regla es la siguiente:
-El prefijo D o L indicará que el grupo -OH está en el último centro quiral de la molécula
En el caso de la glucosa, es el carbono 5, que tiene cuatro centros quirales
Para determinar los centros quirales simplemente consideramos el número de átomos de carbono que existe entre el grupo -CHO y el grupo -CH2OH
El primero de ellos se ubica en la parte superior, en el carbono que sigue al grupo -CHO, y el último en la parte inferior de la molécula, antes del grupo –CH2OH
Por ejemplo:
-Las aldotetrosas, con 4 átomos de carbono, tienen dos carbonos quirales; las aldopentosas tienen 3 y las aldohexosas, tienen 4

