Las reacciones de oxidación-reducción en el ambiente en Temas Selectos de Química 2
Entre los 20 y 50 km por encima del nivel del mar, en la zona de la atmósfera, existe una capa donde se concentra casi todo el ozono atmosférico, por lo cual es común llamarle capa de ozono
Las concentraciones de ozono en esa capa, rondan alrededor de las 10 partes por millón (ppm), lo cual pudiera parecer una pequeña cantidad; sin embargo si tuviéramos este nivel de concentración de ozono al nivel de la superficie ocasionaría graves daños a los seres vivos; pero dada la altura donde se ubica la capa de ozono, esta no es dañina, sino todo lo contrario, resulta de una importancia primordial al sanar de filtro para las peligrosas radiaciones ultravioletas del Sol
Un ejemplo de una reacción redox, es el proceso de formación del ozono, donde por efecto de la luz ultravioleta se rompe la molécula de oxígeno para dar lugar a dos radicales libres:
Los enlaces de la molécula de oxígeno se rompen al absorber energía de un fotón de radiación ultravioleta de longitud de onda menor a 240 nanómetros (nm) y se forman dos átomos de oxígeno libres
Cada uno de estos átomos es tremendamente reactivo y al encontrarse con una molécula de oxígeno reacciona para formar una molécula de ozono
Es importante mencionar que esta reacción se lleva a cabo con la intervención de una molécula, a la que comúnmente se le llama M, y que no se consume en la reacción
Considerando que a la inversa, en el proceso de destrucción, las moléculas de ozono absorben radiación ultravioleta con longitud de onda menor a 320 nm y se rompen en moléculas y átomos libres de oxígeno
El oxígeno reacciona con más ozono para dar lugar a la formación de dos moléculas de oxígeno:
Hay que considerar otras reacciones redox de importancia, las cuales se desarrollan en el medio ambiente y están relacionadas con el problema de la contaminación del aire
Por ejemplo:
-Una nube tóxica contaminante
–Debido a los escapes de los automóviles y a las emanaciones de las industrias instaladas en la ciudad, puede envolver toda una ciudad
La contaminación crónica del aire una ciudad se puede intensificar por una inversión térmica, el cual es un fenómeno atmosférico particular en el cual una masa de aire frío está atrapada bajo una de aire caliente
El dióxido de azufre y los óxidos de nitrógeno (se representa como NOx) son productos todos ellos de las actividades humanas, se liberan a la atmósfera donde se convierten con el concurso de la humedad ambiental y la luz solar, en dos materiales corrosivos en extremo:
-Ácido sulfúrico (H2SO4)
-Ácido nítrico (HNO3)
Estos ácidos se disuelven en las gotas de agua de la atmósfera o en los cristales de hielo y regresan a la tierra en forma de lluvia ácida
Las reacciones implicadas en este fenómeno son: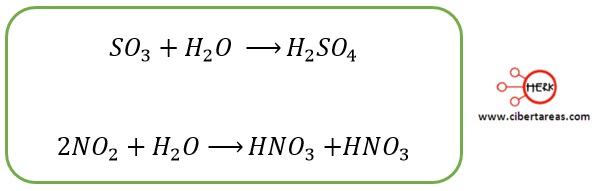
De las dos reacciones anteriores, la segunda es del tipo redox

