Reacciones químicas en la contaminación ambiental – Química 2
Debemos conocer que la contaminación ambiental está estrechamente ligada con la química, ya que al conocer sobre los distintos tipos de contaminantes, sus características y las reacciones químicas que producen, puede ayudarnos a vivir en un mundo más limpio
La atmósfera es una especie de capa protectora que permite la existencia de la vida en La Tierra, también es un medio en el que tienen lugar un número muy variado de reacciones químicas y un número muy variado de reacciones químicos, los cuales producen una serie de contaminantes que afectan el aire, el agua y el suelo
Aire
Se hablan de contaminación atmosférica cuando:
Es muy importante saber que si estas sustancias ponen en peligro la salud humana ya se habla de agentes contaminantes
Reacciones químicas que se producen por la presencia no natural de agentes contaminantes
Monóxido de carbono (CO)
-De forma natural se origina por la oxidación del metano (CH4)
-Este gas se obtiene por la descomposición de la materia orgánica
-La reacción del metano con una pobre cantidad de oxigeno produce una combustión incompleta: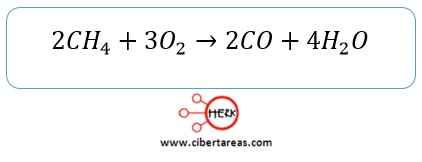
-La principal fuente antropogénica del monóxido de carbono es la combustión incompleta de hidrocarburos, que pueden presentarse en forma de octano (C8H18), uno de los componentes de la gasolina
-Para que la combustión pueda darse adecuadamente se requiere suficiente cantidad de oxigeno
-Como ejemplo podemos mencionar a un auto, la combustión adecuada se logra cuando está bien afinado y la mezcla de gasolina y aire es la adecuada
-Esta es la razón por la cual en muchos países, se exige mediante la verificación vehicular, que la emisión de este contaminante se encuentre en niveles bajos
Óxidos de nitrógeno (NOx)
-La fuente natural del NO2, se encuentra en:
-Descomposición bacteriana de nitratos orgánicos
-Actividad volcánica
-Incendios forestales
-La fuente antropogénica se concentra en la emisión de los gases de los automotores y en la quema de combustibles fósiles
-El monóxido de nitrógeno de la atmósfera reacciona fotoquímicamente con el oxígeno y se convierte en dióxido de nitrógeno, uno de los agentes causantes de la lluvia ácida y el esmog en las ciudades
-También afecta la capa de ozono
-El monóxido de nitrógeno es inofensivo, pero el NO2, es capaz de penetrar profundamente en los pulmones y dañar el sistema respiratorio al modificar su pH
-El NO2, puede causar:
-Bronquitis
-Neumonía
-Susceptibilidad a infecciones virales (gripe)
-Alteraciones del sistema inmunológico
Dióxido de azufre (SO2)
-El SO2 afecta el sistema respiratorio
-Se manifiesta entre las personas que sufren asma y bronquitis crónica
-Los peores efectos se tienen cuando el SO2 reacciona con la humedad del aire para contribuir, mediante una serie de reacciones, a la formación de la lluvia ácida que impacta fuertemente las fuentes de agua, lo cual genera serios trastornos en la vida acuática y silvestre asociada a ellas
Hidrocarburos
-La gasolina contiene una mezcla de hidrocarburos, principalmente:
-Heptano C7H16
-Octano C8H16
-A estos hidrocarburos se les acostumbra adicionar compuestos oxigenados como éteres y alcoholes
-La principal fuente de saturación de hidrocarburos en la atmósfera, son los vehículos así corno también la evaporación de gases
-Los hidrocarburos ocasionan:
-Perdida de coordinación motora
-Náuseas
-Daños en el hígado
-Algunos son potencialmente carcinógenos para humanos y animales
Oxidantes fotoquímicos
-Su mecanismo de formación se realiza por una serie de reacciones químicas y su proceso completo puede ser simplificado en las tres siguientes etapas: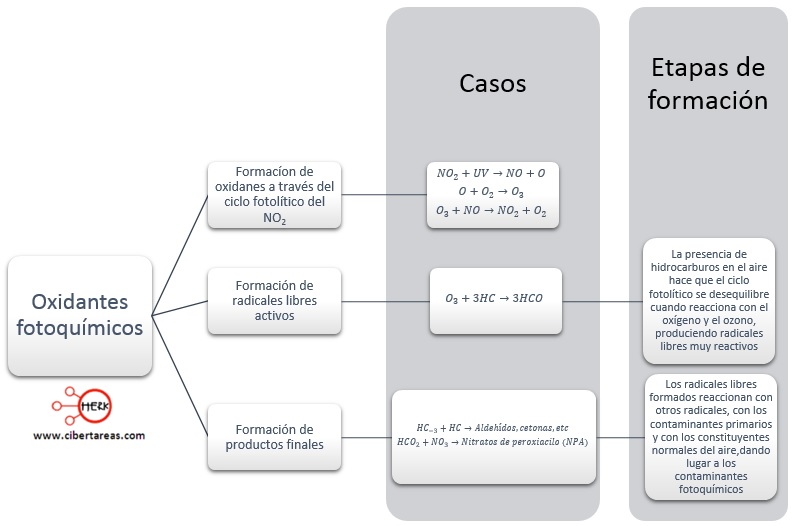
Es importante saber que los nitratos de peroxiacilo son extremadamente tóxicos, a tal grado que se ha determinado que en una concentración de tan solo 0.001 ppm (partes por millón) causan:
-Irritaciones en los ojos
-Irritaciones en los alvéolos pulmonares
-Daños en las cosechas
La presencia del ozono en la atmósfera se relaciona con dos de sus propiedades principales:
-Su alta capacidad para absorber la radiación ultravioleta
-Poder oxidante
La capacidad para absorber la radiación ultravioleta es necesaria para mantener la vida del planeta, ya que funciona como un escudo que impide el paso de los peligrosos rayos ultravioleta (UV) los cuales pueden ocasionar diferentes lesiones a los seres vivos, como mutaciones genéticas.
La segunda propiedad, representa un severo peligro por su presencia en la troposfera, donde se considera uno de los principales contaminantes secundarios, ya que su aparición depende de algunos de los contaminantes primarios, como los óxidos de nitrógeno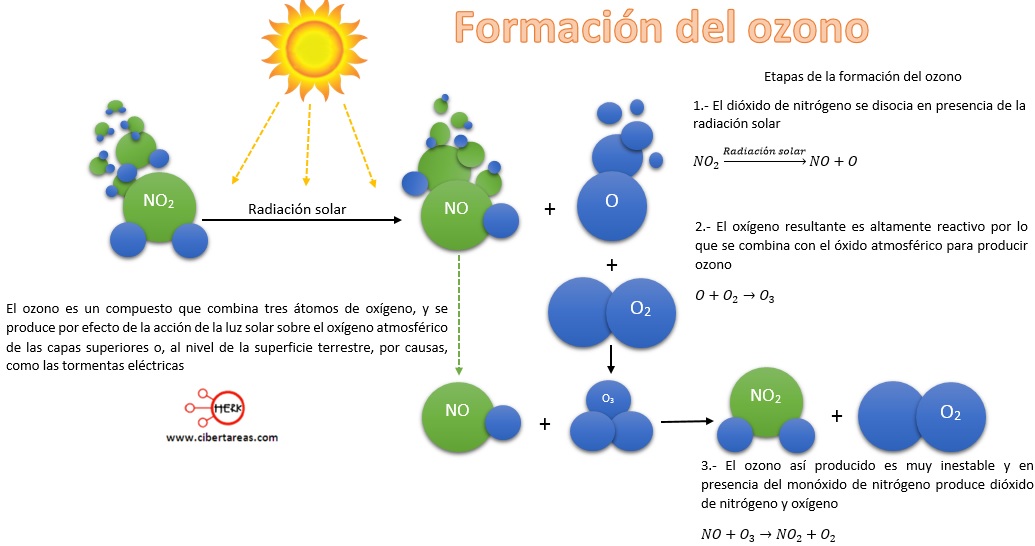
Cuando existe poca o nula actividad humana, los niveles de ozono en la troposfera no alcanzan un valor crítico, sin embargo, cuando hay altos niveles de NO2 y cantidades importantes de hidrocarburos, estos reaccionan con el NO y así surge una alta acumulación de ozono
Para prevenir el daño del ozono se debe disminuir la producción de:
-Óxidos de nitrógeno
-Trazas volátiles de hidrocarburos o las PST
Debido a su alto poder oxidante, el ozono puede incidir sobre la salud humana, y si la exposición es prolongada puede provocar inflamaciones en los bronquios y en las vías respiratorias
Agua
Los contaminantes del agua se pueden clasificar en:
Ejemplo de reacciones químicas que se produce con la contaminación de agua:
-Contaminantes orgánicos disueltos o dispersos en el agua y que provienen de desechos domésticos, agrícolas, industriales y de la erosión del suelo
Los contaminantes orgánicos se descomponen en presencia de oxígeno y liberan energía mediante un proceso denominado aerobiosis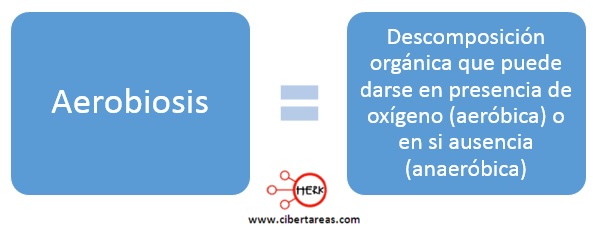
Por ejemplo, la aerobiosis de la glucosa puede representarse mediante la siguiente ecuación: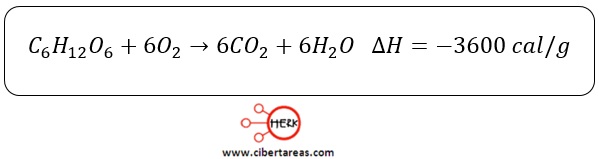
Cuando se agota la materia orgánica que contamina el agua, la acción bacteriana de la desoxigenación de las aguas contaminadas oxida al ion amonio, proceso denominado:
-Nitrificación
Se puede representar mediante la ecuación química iónica, en la que el ion amonio (NH4+) reacciona con el oxígeno para producir iones hidrógeno (H+), iones nitrato (N03) y agua
En los canales y ríos que transportan aguas negras, producto de los desechos urbanos e industriales, es frecuente percibir un terrible olor a “huevo podrido”, que no es otra cosa que el sulfuro de hidrógeno (H2S) obtenido por la putrefacción de las proteínas
La ecuación química correspondiente sin balanceares: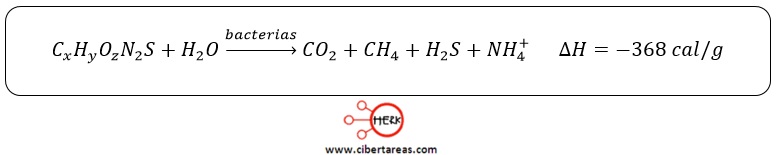
El sulfuro clde hidrógeno es un gas incoloro y muy tóxico, el cual en concentraciones de 5% es nocivo para la vida, por lo que desprende olor fétido
Los peces y otros animales que requieren del oxígeno no pueden vivir en aguas contaminadas donde ocurre la putrefacción
Suelo
El suelo es la mayor fuente de producción de alimentos y el receptor de grandes cantidades de contaminantes, los contaminantes añadidos al suelo contribuyen también a la polución del agua y el aire, por este motivo, el suelo es un elemento clave en los ciclos ambientales
Las principales reacciones químicas que tienen lugar en el suelo, y que involucran a los elementos que constituyen los nutrientes de las plantas, se consideran contaminantes del suelo a algunas sustancias cuando se manejan en exceso o con falta de cuidado
Por ejemplo, los fertilizantes son, en muchos sentidos, necesarios para obtener mejores cosechas, sin embargo, su uso excesivo y sin control acarrea graves problema
En varios países, los fertilizantes más utilizados son los que se fabrican a base de urea (CO(NH2)2) ya que son una fuente para:
-Obtención de nitrógeno
-Elemento esencial para el crecimiento de las plantas y la síntesis de la clorofila
-Incremento de proteínas en los vegetales
-Aumento en la cantidad de hojas y tallos
Cuando la urea se agrega a un suelo con pH mayor a 6.3, esta sufre un proceso de hidrólisis que genera como productos de la reacción amonio (NH4+) y el ion bicarbonato HCO3-1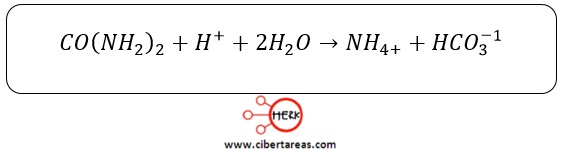
La cantidad de materia orgánica y de líquido “edáfico” son factores a tomar en cuenta para agregar la cantidad apropiada de urea
Cuando se agrega en exceso a las semillas se suele dallar o inhibir su germinación, puesto que el amoniaco en grandes cantidades, se convierte en un tóxico importante
Otros ejemplos de contaminación en los suelos, son los pesticidas, insecticidas y herbicidas, estos sufren una descomposición química que está en función de su estructura y de los grupos activos presentes en la molécula.
Los procesos de óxido-reducción y de hidrólisis o fotólisis son los que se presentan con más frecuencia y estos, a su vez, están fuertemente condicionados por:
-El pH
-La temperatura
-La cantidad de lluvia que recibe el suelo, y su presentación, dado que los pesticidas, herbicidas e insecticidas líquidos son más susceptibles de degradación que los que se presentan en formas sólidas


Julio Javier Perez Paredes says:
Esta magnifico el curso para asimilar conocimientos acerca de esta materia los felicito y les deseo un hermoso y los buenos deseos se cumplan en este 2018
su amigo Julio Javier El Refugio,Oax.68410. MÉXICO
carlos says:
muy bueno
Yolanda buitrago says:
Excelente material
Haydee says:
Es un material muy útil en la actualidad porque necesitamos saber ¿Cómo mitigar la contaminación ambiental que agresivamente se incrementa? La concientización mediante el conocimiento podría sensibilizar a muchos. Los felicito.