Velocidad de reacción – Química 1
Vamos a analizar un ejemplo:
-Consideremos que existe una reacción donde intervienen las sustancias C yD2
-Esta reacción debe producir el compuesto CD
Entonces tenemos que:
Al analizar esta reacción, podemos mencionar que conforme la reacción se va desarrollando, los reactivos C y D se van consumiendo y el producto CD se va formando.
La identificar la concentración de cada sustancia que esta involucrada en la reacción, se representa o se identifica por el símbolo o formula encerrado entre corchetes “[ ]”
El cambio de concentración del producto se expresa mediante la expresión:
La velocidad de desaparición para cada uno de los reactivos, se expresa de manera similar, lo que cambia es un signo negativo, ya que su concentración va disminuyendo conforme transcurre la reacción, tenemos que:
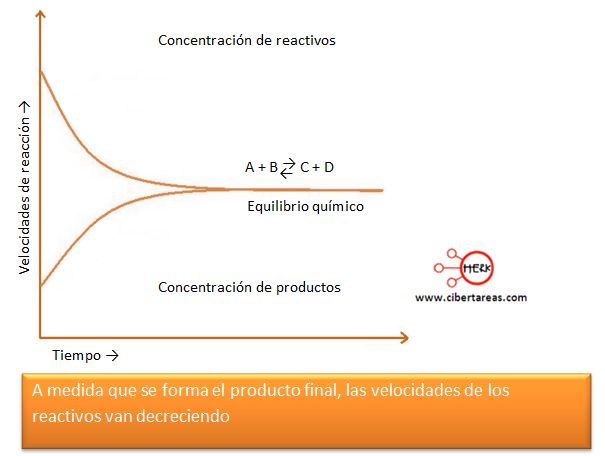
Al graficar el cambio de concentración de productos y reactivos, podemos observar una gráfica como:
Es importante señalar, que no todas las reacciones químicas se desarrollan en la misma velocidad, podemos mencionar el caso de la dinamita, es casi instantánea su verificación y con una gran liberación de energía, y por el contrario tenemos la oxidación de un tornillo de hierro, este puede llevar días o meses enteres en verificarse.
Debemos considerar que para que una reacción química se lleve a cabo no solo basta con solo poner en contacto los reactivos, por ejemplo, al encender un fosforo o cerillo se necesita producir la chispa inicial y la combustión se lleva a cabo por sus propios medios, existen otro tipo de reacciones como la descomposición del clorato de potasio para la producción de oxígeno y cloruro de potasio, esta reacción requiere de que se le suministrase constantemente calor para que pueda desarrollarse.
Para que una reacción pueda efectuarse es necesario proporcionarle un impulso, a este impulso se le conoce como energía de activación (Ea)