Bloques s, p d y f de la tabla periódica – Química 1
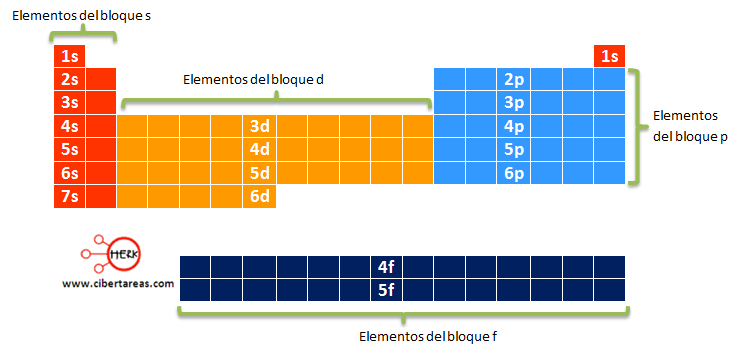
Actualmente la tabla periódica se organiza en grupos y periodos, y se subdivide en cuatro bloques, s, p, d, y f, dependiendo del último orbital de la configuración electrónica.
Para entender de mejor manera como se logra ubicar los elementos en un blique determinado, vamos a analizar el siguiente ejemplo:
Grupo IA (1)
Metales alcalinos: Li, Na, K, Rb, Cs, Fr
Veamos la configuración electrónica para cada uno de ellos:
Como se observa, estos elementos presentan una configuración electrónica similar en su último nivel, ya que todos y cada uno tienen su electrón más externo en un orbital s, y esta es la razón por la cual se ubican en el grupo IA.
Es preciso recordar que el nivel energético equivale numéricamente al periodo en el cual se ubica dentro de la tabla.
Ahora vamos a analizar el aluminio
Numero atómico 13
Configuración electrónica:
Al observar esta configuración, nos indica que los electrones del aluminio se ubican en tres distintas capas o niveles de energía.
Observemos que el aluminio tiene un total de tres electrones, estos están ubicados en la última capa (3s2 3p1), a partir de estos datos se puede afirmar que el aluminio se ubica en el periodo tres, ya que los electrones están en el tercer nivel de energía, se ubica en el grupo III, esto es porque tiene 3 electrones en su última capa y pertenece a un grupo tipo A porque los electrones de la última capa se ubica en orbitales s y p. El aluminio está en el grupo IIIA, periodo tres y bloque tres, para poder ubicarlo en el bloque determinado solo se necesita saber en qué tipo de orbital queda situado el electrón diferencial.
Si se conoce la configuración electrónica de un elemento, se puede determinar el grupo, el periodo y el bloque en los que se ubica en la tabla periódica.





Susana Salcedo Fernandez says:
Buena presentación, creativa, argumentación clara y cientifica de las regiones o bloques en la tabla periodica de los elementos químicos.