El neutrón. James Chadwick – Química 1
Al ser descubierto el núcleo, los científicos tuvieron la curiosidad de saber de qué más estaba formado, y siguieron los experimentos para averiguarlo.
Rutherford dijo que el electrón es 1 836 veces más ligero que el protón, entonces la masa del electrón es casi depreciable y por consecuencia el protón es el que determina en mayor medida la masa del átomo.
Algunos datos recabados de experimentos con relación a la masa de los átomos no concordaba con esta afirmación, ya que si el átomo es neutral, entonces debe existir la misma cantidad de protones que de electrones, y si los protones determina la masa, entonces la del átomo no coincidía con la suma de la masa de los protones y electrones, en otras palabras hacía falta masa.
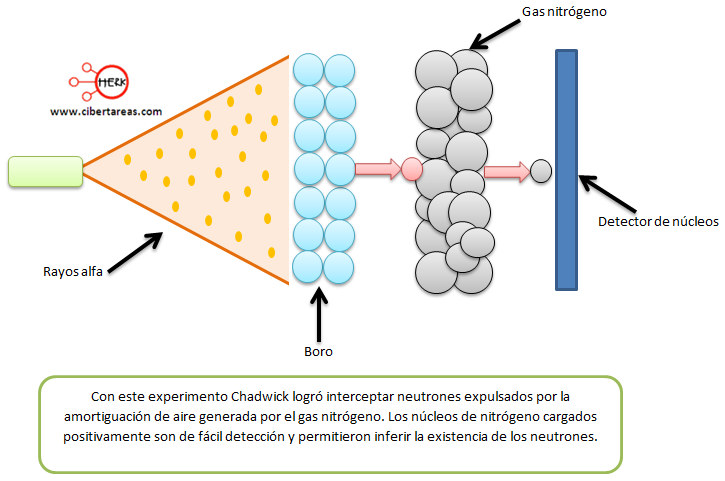
Chadwick realizo sus experimentos en los cuales bombardeo átomos de boro con partículas alfa y a partir del incremento de masa del nuevo núcleo, calculo que la partícula añadida al boro tenía una masa más o menos igual al protón, pero la partícula en si no podía detectarse.
Chadwick explico que esto se daba porque la partícula no poseía carga eléctrica.
Chadwick, llego a la conclusión de que había surgido una partícula nueva, que tenía aproximadamente la misma masa del protón pero sin carga, la definió como electrónicamente neutra.
La nueva partícula descubierta por Chadwick, dio solución a ciertas dudas que los físicos tenían acerca del modelo del núcleo protón – electrón, este descubrimiento completo la estructura del átomo.



SEbaSTiaN streithorst says:
seria mejor que muestres el modelo atomico de chadwick abrazos hazlo gracias!!!
sandra says:
buenaso
chevereeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeeee,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,
Fer says:
Gracias!!!