Estructura de Lewis – Química 1
Tenemos que los electrones de valencia (electrones del nivel más externo de un átomo) son lo responsables directamente de la actividad electrónica que ocurre cuando se da la formación de enlaces químicos.
Para mostrar este hecho, se utiliza las estructuras de Lewis:
Entonces tenemos que la cantidad de puntos colocados alrededor del símbolo químico del grupo A, es igual al número de electrones s y p en el nivel externo de energía del átomo.
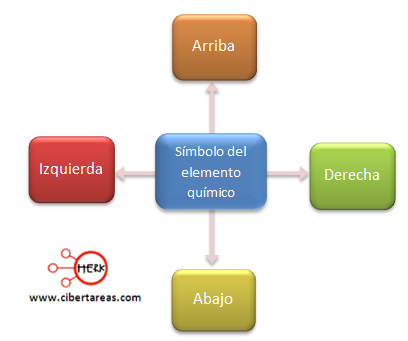
Los puntos se van acomodando alrededor del símbolo del elemento químico, suponiendo que existen cuatro lados o costados:
Dependiendo del número total de electrones del elemento químico, puede darse el caso de que quede uno o más electrones en solitario.
Ejemplos:
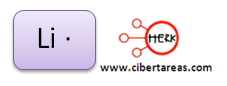
Elemento: Litio (3Li)
Configuración electrónica:
Observemos que este elemento posee dos capas y en la más externa (2s) tiene solo un electrón.
Representándolo con la estructura de Lewis tenemos que:
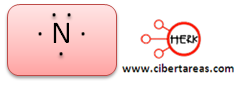
Elemento: Nitrógeno (3N)
Configuración electrónica:
Observemos que este elemento cuanta con un par de electrones apareados y tres que no lo están, están solitarios, estos electrones son los que tendrán la capacidad para participar en el enlace químico.
Aplicando la estructura de Lewis tenemos que:
Elemento: Cloro (17Cl)
Configuración electrónica:
Este elemento en la capa más externa tiene siete electrones, los cuales se distribuyen en tres pares de electrones y un electrón no apareado o solitario.
Al representarlo con la estructura de Lewis tenemos:







samuel says:
esta perfecta esta pagina me ha ayudado mucho con mis tareas