Regla del octeto – Química 1
Gilbert N. Lewis, interpreto la teoría del enlace covalente (formado por un par de electrones compartidos), propuso a su vez la regla del octeto.
En sus experimentos observo que los elementos denominados gases nobles o inertes, difícilmente podrían formar compuestos con otros elementos y además tenían una gran estabilidad.
Al analizar las estructuras electrónicas de estos gases, pudo comprobar que todos poseen 8 electrones en su mapa más externa a excepción del helio.
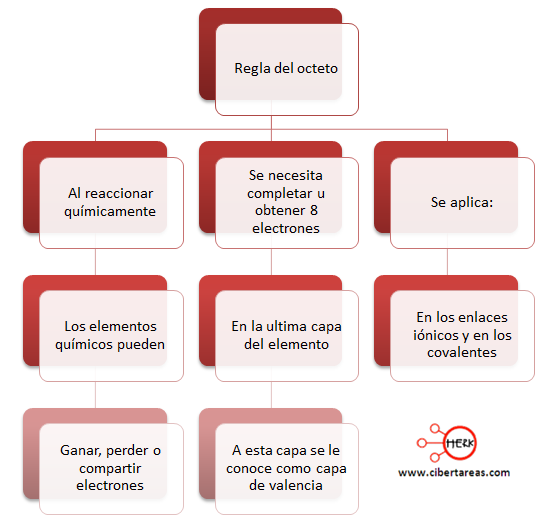
Tenemos que la mayoría de los elementos distintos a los gases nobles reaccionan químicamente, con esto pueden ganar, perder o compartir electrones hasta que se obtengan 8 electrones en la última capa (capa de valencia). Este proceso se le conoce como la regla del octeto.
Los electrones que están ubicados en la capa de valencia, con los que participan directamente con la formación de los enlaces químicos.