Número cuántico l Arnold Sommerfeld – Química 1
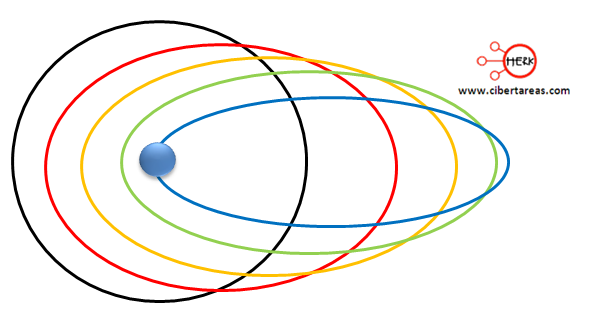
Sommerfeld propone una corrección y menciona que las orbitas además de circulares, podían ser también elípticas, también menciono que donde se observaba un único nivel energético exista, en realidad varios subniveles correspondientes a orbitas ligeramente diferentes.
Bohr, podía definir el radio de una órbita circular con el número cuántico n, pero para poder definir una elipse se necesitan por lo menos dos radios, con esto se necesitan al menos dos números cuánticos más.
Sommerfeld propone un número cuántico l, este número determina un número mayor de orbitas diferentes.
Luis Brogile, señalo que los electrones tiene tanto propiedades de onda como de partículas, con esto entendemos que existe una dualidad, donde todas las que habían sido consideradas com partículas (electrones, protones, neutrones) también podrían tratarse como modelos ondulatorios, este postulado se confirmó con los experimentos donde se logró difractar electrones como si fueran un haz de luz.
Con este comportamiento de dualidad de los electrones, se dio el origen del principio de Werner Heinsberg, el cual es:




Paula Flora Aniceto VATGAS says:
La iniciativa de compartir los conocimientos con la sociedad es genial