Coloides – Química 2
El nombre coloide proviene de:
Los sistemas coloidales están presentes en la vida diaria:
-Higiene personal
-Jabones
-Shampoo
-Pasta dental
-Crema de afeitar
-Cosméticos
-Alimentos
–Leche
-Mantequilla
-Cremas vegetales
-Mermeladas
-Naturaleza
-Neblina
-Efectos en el cielo que le hacen tener diversos colores
-Productos o bienes de consumo
-Agua potable
-Algunos procesos de separación en las industrias
-Biotecnología y el medio ambiente
Debemos mencionar que también son importantes los coloides biológicos como:
-La sangre
-Humor vítreo o cristalino que se encuentra en el interior del ojo, etc.
En una disolución, las partículas son de tamaño molecular, mientras que en el caso de las dispersiones coloidales, las partículas son más grandes, pero no tanto como para asentarse por efecto de la gravedad, como sucede en las suspensiones
Es importante saber que la partícula coloidal puede consistir en muchos átomos, iones o moléculas, pero también puede ser una molécula gigante, los tamaños moleculares, para este tipo de partículas, se han medido en unidades de nanómetros (nm), aunque también se puede hacer una primera distinción entre ellas tres, pues las suspensiones se caracterizan por asentarse en el fondo de las disoluciones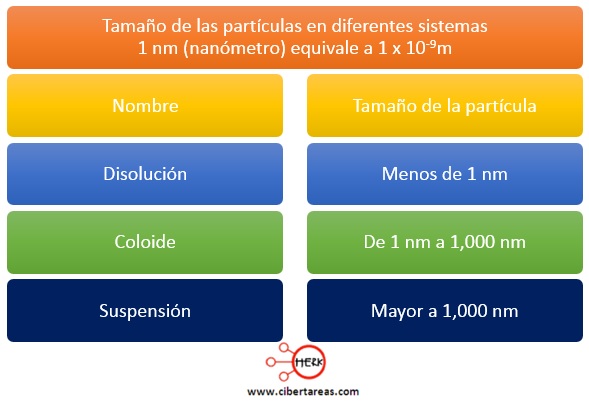
Otro aspecto a considerar es que los coloides se clasifican tomando en cuenta el estado físico de la fase dispersa y de la fase dispersora: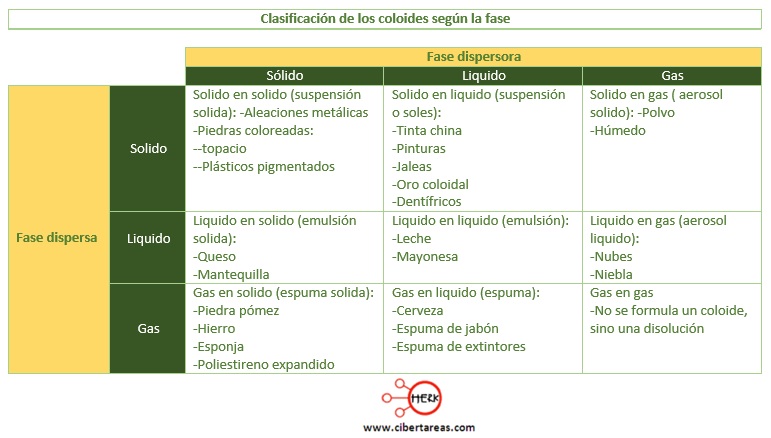
Otra forma de clasificar a los coloides:
Coloides hidrófilos
-Son de naturaleza orgánica
-Sus moléculas están constituidas por una larga cadena hidrocarbonada con un grupo polar en uno de los extremos
-Se disuelven en agua, ya que se forman enlaces de hidrógeno entre el grupo polar y las moléculas de agua
-No son solubles cuando la parte hidrocarbonada es larga, pues no son atraídas por las moléculas de agua
-Estas dos fuerzas opuestas hacen que las moléculas se agrupen en pequeñas partículas, de tal forma que los grupos polares se orientan hacia la superficie y las partes hidrocarbonadas hacia el interior de las partículas
Esto sucede con algunas proteínas que tienen en sus extremos coloides hidrófilos y se agrupan de tal forma que los coloides hidrófobos se encuentran al interior de la molécula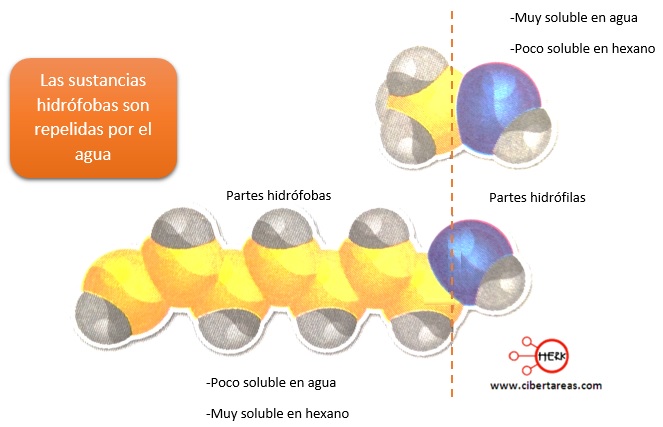
Las partículas coloidales pueden ser tan pequeñas que la dispersión puede aparecer uniforme incluso bajo un microscopio, pero al mismo tiempo son lo suficientemente grandes para dispersar un haz de luz que pase por su interior y por ello es que las dispersiones coloidales tienen un aspecto turbio o lechoso, salvo que se encuentren muy diluidas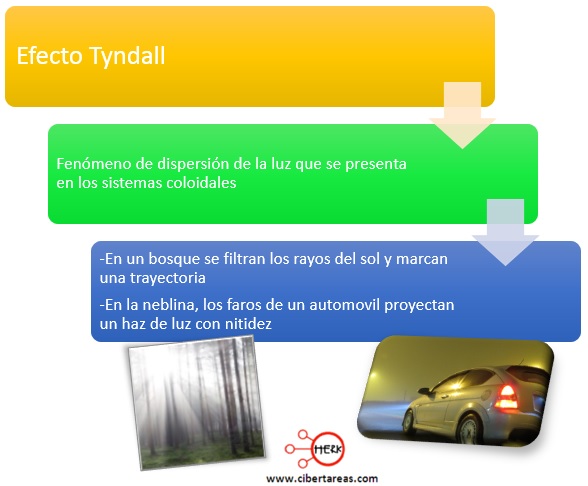
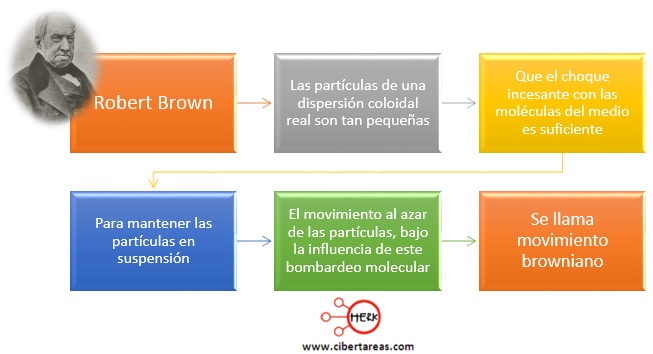
Este movimiento se descubrió cuando Brown preparó una suspensión acuosa de granos de polen y al revisarla bajo el microscopio observó que los granos presentaban un movimiento errático, caótico e incesante
Llegó a pensar que tal movimiento podía deberse a que el polen se encontraba vivo, sin embargo, cuando probó con polen conservado durante siglos volvió a observar exactamente el mismo movimiento
Este movimiento constante se da porque al estar inmersas en un fluido, también reciben insumos energéticos de parte de las moléculas del fluido que son sometidas a una agitación térmica

