Osmosis – Química 2
Debemos sabe que el fenómeno de la ósmosis deriva de:
-La evolución de los sistemas unicelulares, que desarrollaron una membrana que les permitió un eficaz intercambio de material con los alrededores
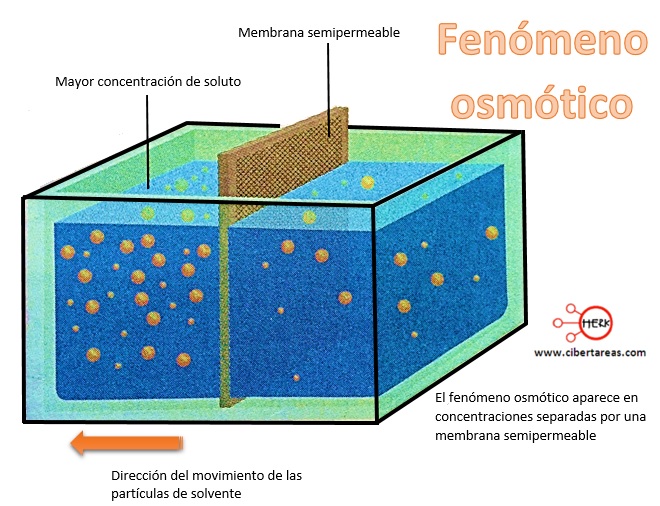
El fenómeno osmótico fue descubierto por el fisiólogo y físico francés Henri Dutrochet, su propuesta dice que:
Tenemos que el flujo de solvente se efectúa desde la solución diluida a la solución con mayor concentración y a través de la membrana semipermeable; este proceso permanece hasta que el fenómeno se equilibra y el flujo de solvente es igual en ambas direcciones
Es importante destacas que existe una razón por la cual el sistema alcanza el equilibrio, es porque el flujo de solvente va generando un aumento en la presión hidrostática del lado de la solución concentrada (presión osmótica)
El valor de la presión osmótica depende de variables como:
-La concentración de la disolución
-El volumen
-La temperatura que esta tenga
La relación existente entre estas variables se expresa por medio de la siguiente ecuación: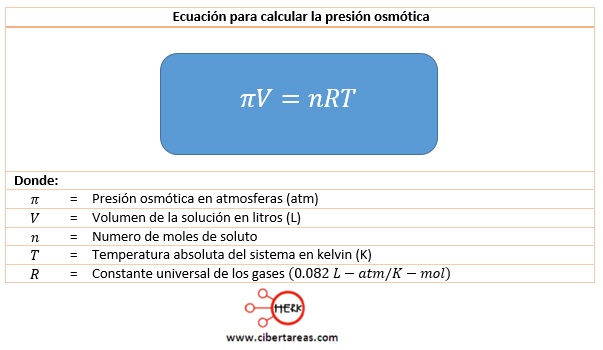
Ejemplo
Problema:
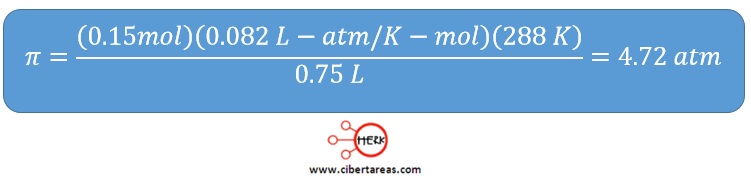
-En una solución donde se ha tenido que disolver 0.15 moles de un soluto para tener un volumen de 750 mL, es necesario determinar el valor de la presión osmótica
-El proceso se desarrolla a presión atmosférica normal y a una temperatura de 15°C
Solución:
-Datos
–=?
–V = 750 mL = 0.75L
–n = 0.165 mol
–T = 15°C + 273 = 288 K
–R = 0.082 L-atm/K-mol
El proceso osmótico puede invertirse si se aumenta suficientemente la presión del lado de la solución concentrada para forzar la salida de solvente hacia donde se encuentra la solución diluida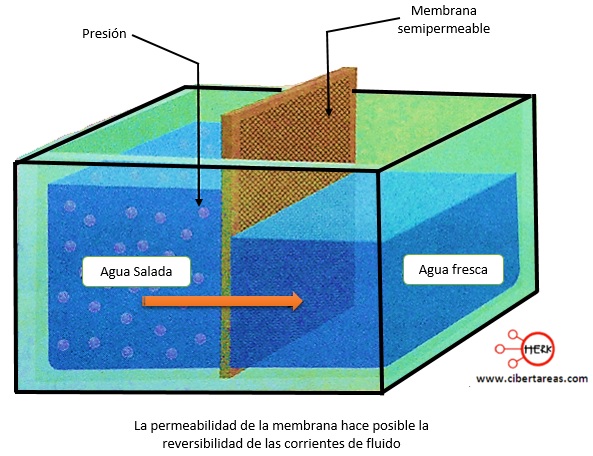
A este proceso se le conoce como osmosis nueva, y se utiliza para impurezas del agua como:
-Solidos disueltos
-Compuestos orgánicos
-Materia coloidal
-Algunos virus
-Algunas bacterias
Mediante la osmosis inversa es posible eliminar de 95 a 99 por ciento de los sólidos disueltos totales y el 99 por ciento de todas las bacterias, lo que proporciona agua con una pureza considerable