La teoría de Arrhenius en Temas selectos de química 2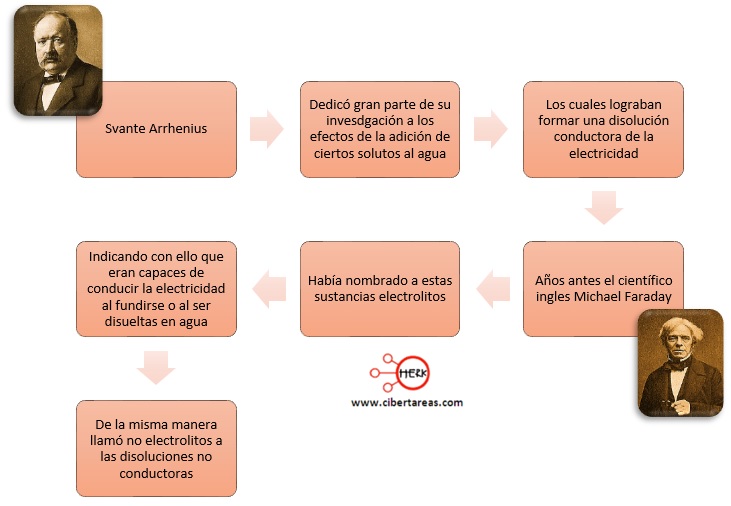
Por ejemplo:
-Una disolución de NaCl en agua es un electrolito porque es capaz, mediante el dispositivo adecuado, de conducir la electricidad a través de ella
-Mientras que una disolución de azúcar no conduce la electricidad y se considera como un no electrolito
En su teoría, Arrhenius considera que:
-Los electrolitos existen en el agua como partículas cargadas eléctricamente (iones) y que una disolución de tales iones deberá contener igual número de iones positivos y negativos
Por ejemplo:
-Al preparar una disolución 0.10 M de NaCl en agua se obtenga una cantidad igual de iones Na+ que de iones Cl–, con lo cual tendremos una concentración 0.10 M de iones sodio y 0.10 M de iones cloruro
Hay que considerar que los electrólitos, tienen un papel importante en las propiedades coligativas, las cuales son: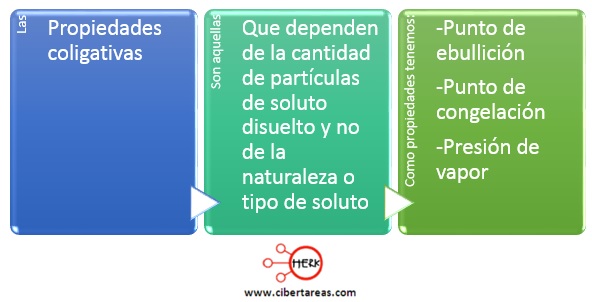
Entonces tenemos que el punto de ebullición, de congelación y la presión de vapor se afectan por la cantidad de iones disueltos
Por esa razón se utilizan como un medio indirecto para determinar hasta qué porcentaje se disocia un electrolito
Teóricamente, electrolitos corno el H2S04, o el NaCI, se disocian al 100% cuando se disuelven en agua
Sin embargo esto no es así en la realidad y aunque se llega a un porcentaje muy alto, queda una parte sin disociarse debido a que, probablemente, se establece un equilibrio dinámico en el que algunos iones vuelven al estado original, al mismo tiempo que tiene lugar el proceso de disolución en el cual el electrolito produce iones
Aunque los ácidos y las bases eran conocidos como tales desde hace muchos años y sus características más generales estaban bien determinadas, sin embargo aún no se había logrado explicar el porqué de su comportamiento peculiar
El mérito de Arrhenius consiste en ser el primer científico en:
-Conocer la naturaleza fundamental de los ácidos y de las bases
A partir de sus experimentos con electrolitos, postuló que:
En primer lugar hay que considerar la acción de cuatro ácidos conocidos:
-Ácido sulfúrico (ácido de acumulador)
-Ácido muriático (que se utiliza como sustancia para quitar el sarro de los baños y otros lugares)
-Ácido acético (ingrediente importante del vinagre)
-Ácido carbónico (que se encuentra en las bebidas gaseosas)
Cada una de estas sustancias es capaz de producir iones hidrógeno en disolución acuosa, por lo cual se les considera a todos como ácidos de Arrhenius:
Debemos saber que las cuatro sustancias mencionadas presentan enlace covalente y que la producción de iones hidrógeno y los aniones respectivos se debe a la acción del agua, que es una sustancia polar
Tanto el ácido acético como el ácido carbónico no se ionizan completamente, por lo que se establece un equilibrio entre los iones hidrógeno, iones acetato y ácido acético, lo cual se expresa mediante la escritura de la doble flecha
Lo qué sucede con las bases: el hidróxido de sodio, el hidróxido de calcio y el hidróxido de aluminio, cuando se disuelven en agua producen iones hidroxilo u oxhidrilos (OH–) y se reconocen como bases de Arrhenius:

