Fuerza de los ácidos y de las bases – Química 2
Los ácidos y las bases se pueden calificar en:
-Fuertes
-Débiles
Los ácidos y las bases se pueden calificar en:
-Fuertes
-Débiles
Johannes N.Brönsted, químico danés, y Thomas Lowry, químico británico, propusieron, cada uno de forma independiente, una teoría que mejora significativamente la propuesta de Arrhenius, ya que esta última se limitaba a las soluciones acuosas y se han encontrado reacciones ácido-base que se verifican en fase gaseosa o en solvente, distintos al agua, como el caso de:
-Amoniaco
-Cloruro de hidrogeno
Estos reaccionan en fase gaseosa para formar una sal, el cloruro de amonio: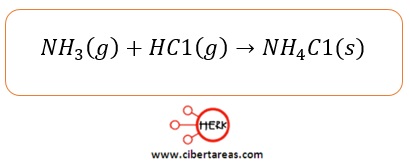
El químico Svante Arrhenius, dedicó gran parte de su investigación científica a los efectos de la adición de ciertos solutos al agua que lograban formar una solución conductora de la electricidad.
Anterior a Svante, el científico inglés Michael Faraday había nombrado a estas sustancias electrolitos, indicando con ello que era capaces de conducir la electricidad al fundirse o al ser disueltas en agua, basándose en sus experimentos con electrolitos, Arrhenius postuló que:
Debemos conocer que la acidez y la basicidad son, desde el punto de vista químico, dos comportamientos contrapuestos de diversas sustancias que llamaron la atención de muchos científicos
El estudio de los procesos químicos en los que intervienen los ácidos y las bases siempre ha ocupado un lugar destacado en la historia de la química; sin embargo, en la química moderna solamente se tenía la descripción de algunas propiedades como:
-Sabor agrio de los ácidos
Textura jabonosa de los álcalis o bases
Pero no se conocían las razones que, a nivel molecular, distinguían a un ácido de una base