Geometría molecular – Química 2
En los compuestos del carbono pueden darse múltiples tipos de geometría, y sus propiedades como:
-Reactividad
-Actividad farmacológica
-Actividad tóxica
-Actividad biológica, etc.
Estas propiedades dependen de su geometría molecular
Los compuestos químicos son tridimensionales y los átomos que los constituyen se acomodan en el espacio de una manera específica, que está influenciada por la naturaleza propia de cada uno y del tipo de enlace que establecen entre ellos
El estudio de la geometría molecular requiere de los conocimientos básicos de las estructuras de Lewis, ya que estas permiten conocer la cantidad de electrones libres y enlazados para cada átomo
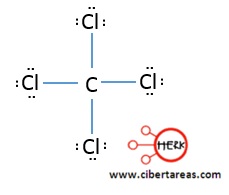
Por ejemplo, el tetracloruro de carbono (CCl4), donde se nota que cada átomo de Cl tiene un electrón desapareado, que forma el enlace con el carbono central
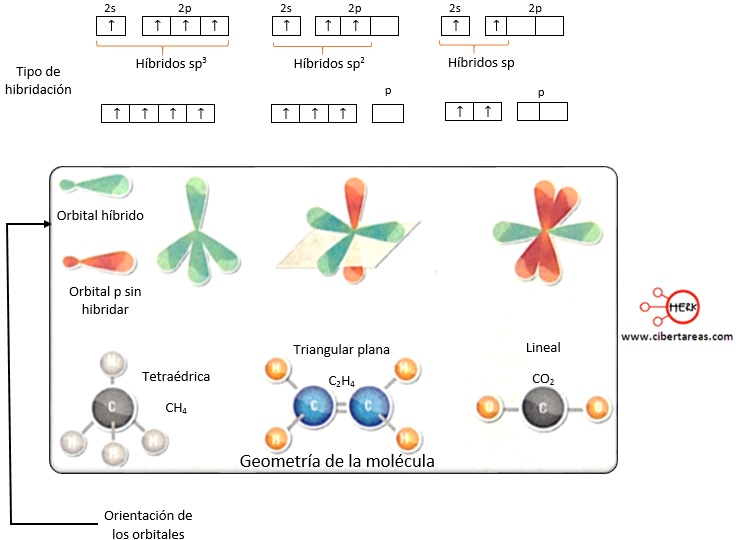
Los compuestos de carbono pueden adoptar tres geometrías moleculares con distintas propiedades:
Tetraédrica
-En esta propiedad, los cuatro orbitales híbridos sp3 del átomo de carbono adoptan una geometría tetraédrica
-Cada uno de estos orbitales forman un ángulo aproximado de 109.5° y se orientan hacia los vértices de un tetraedro
-La hibridación sp3 es propia de los compuestos orgánicos en los que el átomo de carbono presenta exclusivamente enlaces simples, como ocurre en los alcanos
Trigonal plana
-En esta propiedad, la geometría que adopta el átomo de carbono con hibridación sp2 es trigonal plana con un ángulo de 120° entre los orbitales híbridos
-El suborbital p libre se coloca perpendicularmente a los orbitales híbridos sp2
-La hibridación sp2 es propia de los compuestos que presentan doble enlace entre los átomos de carbono, como sucede en los alquenos
Lineal
-En esta propiedad, la disposición espacial de la hibridación sp corresponde a una geometría lineal con una separación de 180° entre los orbitales híbridos
-Los compuestos con hibridación sp presentan átomos de carbono que establecen triples ligaduras, como en el caso de los alquinos