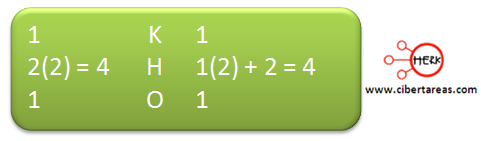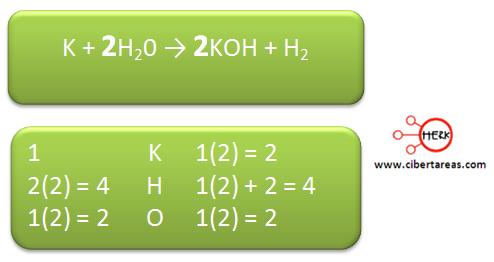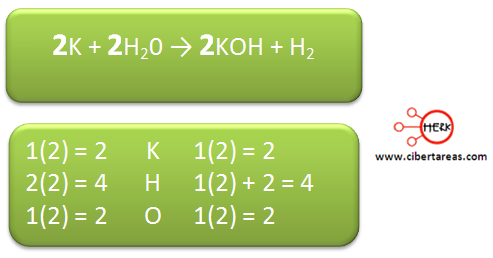Método de tanteo (Aproximaciones) – Química 1
En el método de tanteo, se realizan los siguientes pasos:
Primer ejemplo
Tenemos la siguiente reacción:
Reacción entre le carbono y el ácido sulfúrico, para producir: Dióxido de azufre, Dióxido de carbono y agua.
Ecuación:
Analicemos la solución:
1.- Se cuenta el total de átomos de cada elemento antes y después de la reacción
2.- Podemos observar que solamente existen no metales para el ejemplo, esto hace ver que el oxígeno no está equilibrado, ya que en los reactivos existen 4 átomos, y en los productos existen 5 átomos los cuales están repartidos en 3 sustancias distintas.
Este método está catalogado como un método de ensayo y error, ya que se asigna un coeficiente donde se observa que pueda ser adecuado, y a partir de esto se va equilibrando todos los demás.
Para este ejemplo se va asignar un coeficiente 2 al ácido sulfúrico (H2SO4), con esto se aumentara el número de átomos de oxígeno en el reactivo, así quedaría la fórmula:
Al asignar este coeficiente ahora se tienen en los reactivos:
4 átomos de hidrogeno
2 átomos de azufre
8 átomos de oxigeno
Como consecuencia se puede colocar un coeficiente 2 al dióxido de azufre y otro al agua para ajustar las cantidades respectivas de azufre y de hidrogeno, la formula quedaría así:
Después de esto, se cuentan los átomos y como resultado tenemos:
Con esto, todos los átomos están equilibrados y con esto se tiene la solución.
Segundo ejemplo
Tenemos la reacción:
Reacción entre el potasio y el agua, para producir hidróxido de potasio e hidrogeno.
La ecuación es:
Analicemos la solución:
1.- Es necesario contar los átomos de cada lado de la ecuación
2.- Ahora es necesario ajusta los elementos:
En primer lugar los metales
Después el hidrogeno
Posteriormente el oxigeno
Debido a que los átomos de potasio son numéricamente iguales en los dos lados de la ecuación, se prosigue con el hidrogeno:
Se asignan los coeficientes que se han encontrado pero existe un problema, los otros elementos se han afectado, por esta razón es necesario volver a contar:
Para poder finalizar, es necesario equilibrar los átomos de potasio, para esto se le asigna un 2 como coeficiente:
Con esto, la ecuación ha quedado balanceada y también cumple con la ley de la conservación de la materia.